TECHNIQUES
Éclosion Assistée (Hatching)
L’éclosion assistée (Hatching) est une technique de fertilité, utilisée dans le cadre des traitements de FIV, pour faciliter l’éclosion et le processus d’implantation de l’embryon.
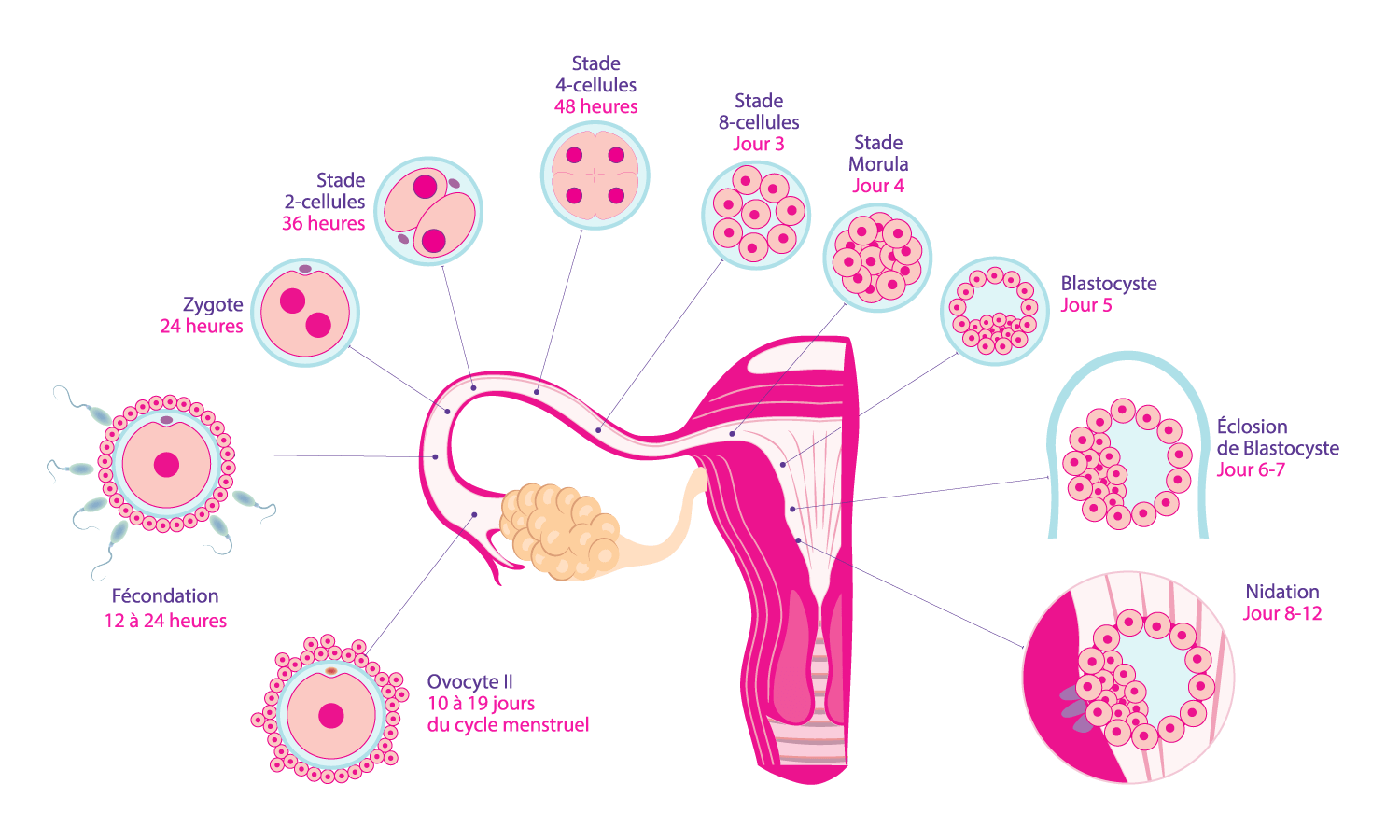
Pour mieux comprendre l’éclosion assistée, il est utile de comprendre le processus naturel d’éclosion d’un embryon (voir ci-dessous: comment les embryons éclosent naturellement)
Pendant le traitement FIV, la fécondation a lieu au laboratoire. Cependant, il faut savoir que le fait d’avoir un embryon fécondé ne garantit pas la grossesse. L’embryon transféré doit s’implanter dans l’endomètre et « coller » pour que la grossesse se produise.
Chez les femmes de moins de 35 ans, le pourcentage d’embryons transférés qui « collent » (taux d’implantation) est de près de 50 %. Pour les femmes de plus de 42 ans, il est inférieur à 10 %.Il y a plusieurs théories sur le défaut d'implantation, et l’une de ces théories est que l’embryon n’éclot pas correctement. Cette absence d’éclosion peut se produire parce que l’embryon possède intrinsèquement une coquille exceptionnellement dure, ou parce que quelque chose dans l’environnement du laboratoire — comme les milieux de culture utilisés pour maintenir l’embryon en vie ou les produits chimiques de cryoconservation (congélation) — a interrompu artificiellement le processus d’éclosion.
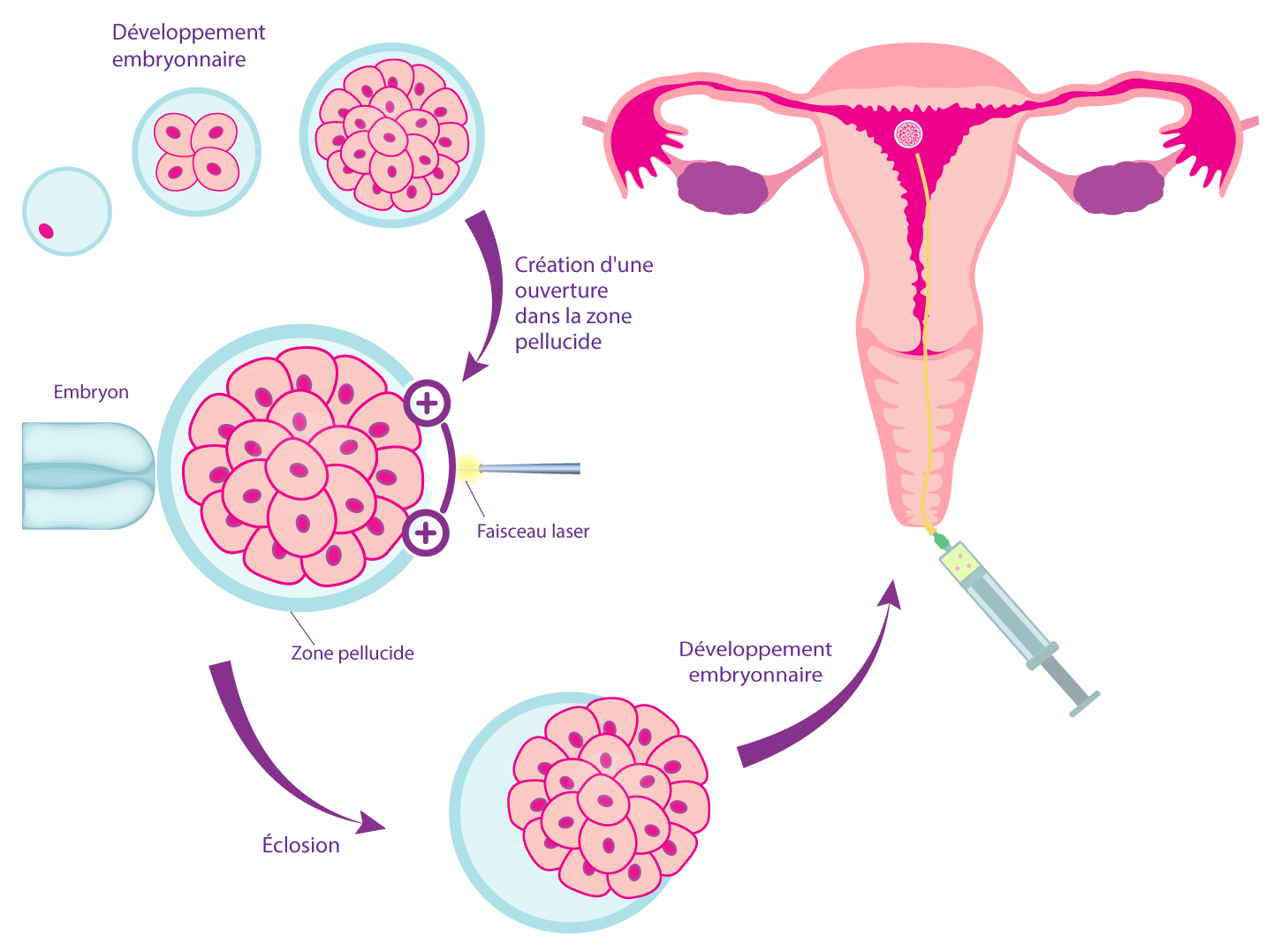
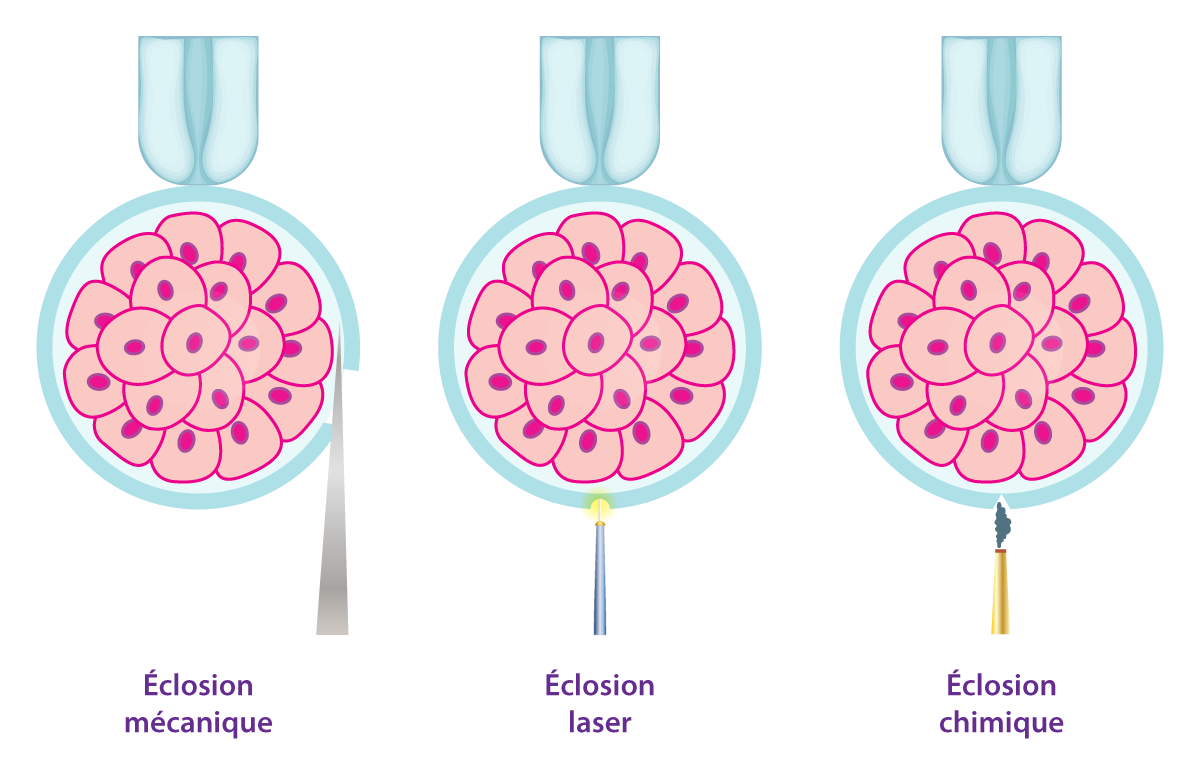
L’éclosion assistée vise à surmonter les obstacles qui empêchent l’éclosion naturelle. Elle essaie d’imiter la nature en amincissant la zona pellucida d’un embryon produit par la FIV, avant qu’il ne soit introduit dans l'utérus. Le principe repose sur le fait que cette éclosion assistée pourra augmenter les taux d’implantation et donc augmenter les chances de tomber enceinte.
L’éclosion assistée (Hatching) est une technique de fertilité, utilisée dans le cadre des traitements de FIV, pour faciliter l’éclosion et le processus d’implantation de l’embryon.
Pour mieux comprendre l’éclosion assistée, il est utile de comprendre le processus naturel d’éclosion d’un embryon (voir ci-dessous: comment les embryons éclosent naturellement)
Pendant le traitement FIV, la fécondation a lieu au laboratoire. Cependant, il faut savoir que le fait d’avoir un embryon fécondé ne garantit pas la grossesse. L’embryon transféré doit s’implanter dans l’endomètre et « coller » pour que la grossesse se produise.
Chez les femmes de moins de 35 ans, le pourcentage d’embryons transférés qui « collent » (taux d’implantation) est de près de 50 %. Pour les femmes de plus de 42 ans, il est inférieur à 10 %.Il y a plusieurs théories sur le défaut d'implantation, et l’une de ces théories est que l’embryon n’éclot pas correctement. Cette absence d’éclosion peut se produire parce que l’embryon possède intrinsèquement une coquille exceptionnellement dure, ou parce que quelque chose dans l’environnement du laboratoire — comme les milieux de culture utilisés pour maintenir l’embryon en vie ou les produits chimiques de cryoconservation (congélation) — a interrompu artificiellement le processus d’éclosion.
L’éclosion assistée vise à surmonter les obstacles qui empêchent l’éclosion naturelle. Elle essaie d’imiter la nature en amincissant la zona pellucida d’un embryon produit par la FIV, avant qu’il ne soit introduit dans l'utérus. Le principe repose sur le fait que cette éclosion assistée pourra augmenter les taux d’implantation et donc augmenter les chances de tomber enceinte.